| |
| 輔助生殖技術(包括人類輔助生殖技術和人類精子庫)是指運用醫學技術和方法對配子、合子、胚胎進行人工操作,以達到受孕目的的技術,分為人工授精技術、體外受精-胚胎移植技術及相關衍生技術【1】。 |
| |
| 其中體外受精-胚胎移植技術及其各種衍生技術(In vitro fertilization, IVF)近些年來備受關注。簡單的說,就是大家耳熟能詳的試管嬰兒技術。 |
| |
| “試管嬰兒”的前世今生? |
| 1978年世界上*試管嬰兒誕生,從此開創了生殖醫學領域的新紀元。 |
| 試管嬰兒是指從女性體內取出卵子,在器皿內培養后,加入經技術處理的精子,待卵子受精后,繼續培養,到形成早早期胚胎時,再轉移到子宮內著床,發育成胎兒直至分娩的技術【1】。 |
| |
| 試管嬰兒技術的分類 |
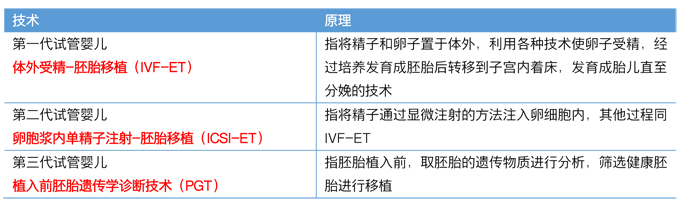 |
| |
| 第三代試管嬰兒的分類 |
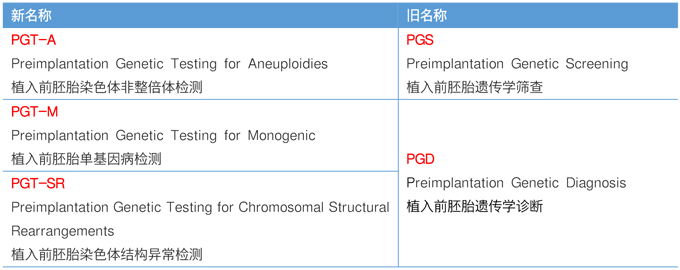 |
| |
| 為什么選擇PGT-A? |
雖然試管嬰兒技術給無法孕育下一代的夫婦帶來了希望,但胚胎染色體數目異常在常規體外受精中較常發生,且高齡女性胚胎染色體異常的發生率更高。
PGT-A技術,對植入前的胚胎細胞進行染色體非整倍體以及染色體拷貝數變異檢測,選擇染色體數目正常的胚胎,可有效提高體外受精的成功率,有助于輔助生殖技術的推廣應用。 |
| |
| PGT-A的研究方法 |
| 前幾年主要通過熒光原位雜交(FISH)技術、比較基因組雜交芯片(aCGH)技術進行PGT-A分析。隨著二代測序(NGS)的快速發展,人們將目光轉向NGS方法,以期進行更正確的評估。 |
| |
| PGT-A研究的難點之一是選擇合適的單細胞全基因組擴增技術 |
| 基于NGS技術進行PGT-A研究時,由于每個胚胎細胞中的DNA非常少(皮克級),遠沒有達到測序所需的樣品量,因此需要先對單細胞內的DNA進行全基因組擴增(whole genome amplification, WGA),而這一過程必須盡可能避免樣本的損失和污染,并盡可能保證擴增的覆蓋度、均一性等,這都是極其困難的,所以選對單細胞全基因組擴增技術很重要! |
| |
| Takara致力于為科學研究提供支持,傾力推出的PicoPLEX技術,目前廣泛用于PGT-A研究。接下來讓我們一起來看一下: |
| |
| PicoPLEX技術是如何正確而高效的進行PGT-A研究 |
| ■ 操作簡便,避免珍貴樣品的損失 |
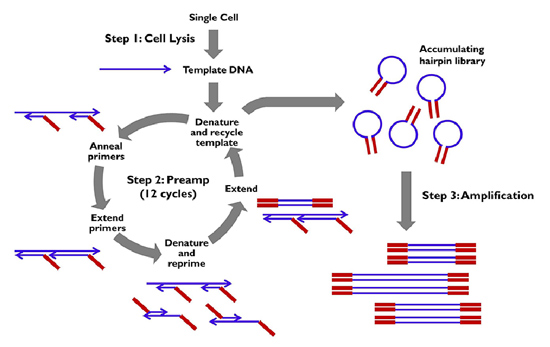
| 整個實驗過程是 “飛一般的感覺”(見下圖),就三小時,就三小時(細胞裂解→預擴增→低背景的PCR擴增),便可獲得微克級的DNA產物。過程中不需要轉管和純化,減少過多實驗操作可能帶來的樣本損失! |
| |
 |
| |
| ■ 炫酷的“準線性預擴增+發夾結構”加持,保證擴增的均一性 |
| 在經過細胞裂解后,以DNA作為模板使用準線性擴增方法進行預擴增,并在每個循環后形成一個不能被進一步擴增的發夾結構,這樣做的好處是有效避免PCR過程中可能引入的擴增錯誤無限放大,避免序列偏向性。 |
| |
| ■ 可用于高品質的染色體變異(CNV)分析 |
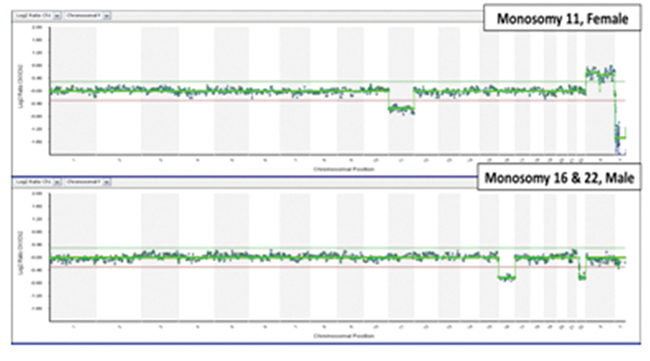 |
| 利用單卵裂球活體組織檢查樣品進行PicoPLEX WGA Kit擴増標記后,與24 sure array雜交,結果清晰地顯示了CNV(上圖)。2011年ESHRE(歐洲人類生殖與胚胎學會)的臨床實驗證明了采用PicoPLEX 技術進行人類染色體核型分析的準確性。 |
| |
| ■ 實例大公開:進行PGT研究時,PicoPLEX性能出色 |
| 來自西班牙Sistemas Genómicos Ltd.的Vendrell【2】的團隊,開發了一種高度可靠的檢測單個卵裂球和5-10滋養外胚層細胞樣品的染色體異倍性的實驗方法。其中使用PicoPLEX試劑盒擴增獲得gDNA產物用于后續NGS分析。實驗表明,未擴增的對照DNA樣品和來自單個卵裂球的WGA產物在測序數據上基本沒有差異,且可以正確地檢測染色體異倍性。 |
| 表明使用PicoPLEX技術具有高再現性,適用于PGT-A分析。 |
| |
| 拓展:無創胚胎植入前非整倍體基因檢測(niPGT-A) |
| 盡管胚胎活檢被認為是一種相對安全的方法,但其他侵入性較小的技術近也受到關注。研究表明,可以通過檢測釋放到培養基中的游離DNA(cfDNA),即無創胚胎植入前非整倍體基因檢測(niPGT-A)來判斷胚胎非整倍體情況。由于cfDNA的含量遠少于侵入式活檢的細胞DNA,因此具有高靈敏度和低偏差的WGA方法對于niPGT-A獲得足夠的材料進行下游分析至關重要。 |
| 來自南加州大學的Jacqueline團隊【3】,通過對廢胚胎培養基(SEM)中提取的cfDNA進行全基因組擴增,分析胚胎染色體的非整倍性,驗證無創胚胎植入前基因檢測非整倍體檢測(niPGT-A)的可靠性。實驗分別對SEM,滋養外胚層細胞和完整胚胎樣本使用PicoPLEX進行WGA,然后利用NGS方法進行PGT-A分析。結果表明,使用63.2 ng/ul的cfDNA足以用于正確的進行染色體異倍性分析,但一致性略低。這也表明,PicoPLEX技術可以提供高質量的基因組DNA, 助力niPGT-A分析。 |
| |
| 更多PicoPLEX技術產品 |
| PicoPLEX® WGA Kit:用于單細胞文庫構建的全基因組擴增解決方案 PicoPLEX® DNA-seq Kit:單細胞 DNA 文庫制備技術,適用于 Illumina 所有 NGS 測序平臺 ThurPLEX® DNA-seq Kit:更高的通量, 更好的性能, 用于所有 Illumina 的 NGS 平臺 |
| |
| 參考信息及文獻來源 |
1. 中華人民共和國國家衛生健康委員會
2. Vendrell, X. et al. New protocol based on massive parallel sequencing for aneuploidy screening of preimplantation human embryos. Syst. Biol. Reprod. Med. 63, 162-178 (2017).
3. Ho, J. R. et al. Pushing the limits of detection: investigation of cell-free DNA for aneuploidy screening in embryos. Fertil. Steril. 110, 467-475.e2 (2018). |
